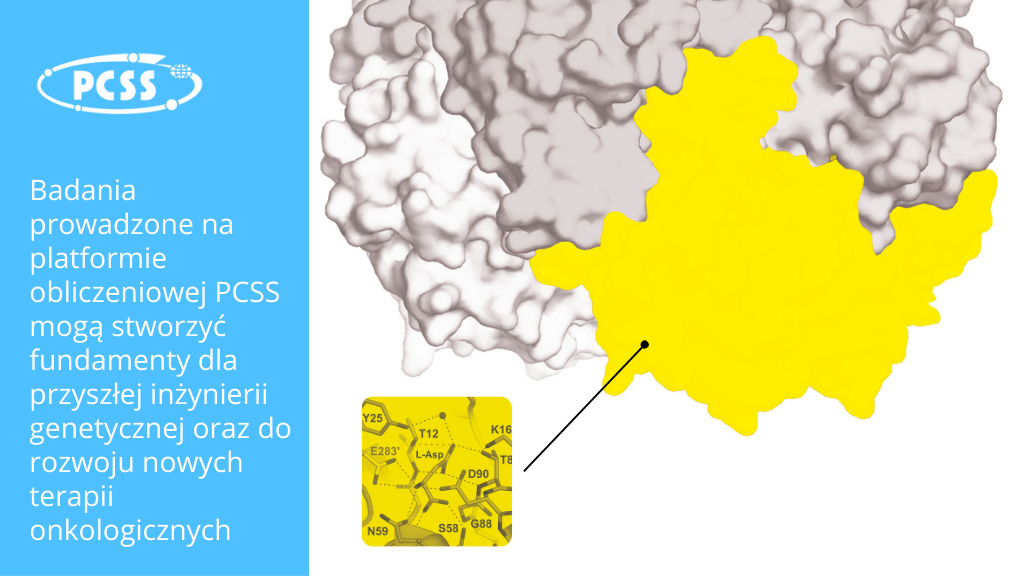
Bazy sekwencji genomowych w połączeniu z wielkoskalową strukturalną analizą in silico mogą skutecznie prognozować właściwości potencjalnych enzymów o znaczeniu medycznym. Poznańskie Centrum Superkomputerowo-Sieciowe pozwoliło zastosować rozwinięte oprogramowanie do analizy ponad 256 mln białek zawartych w 85 tysięcy genomów bakteryjnych.
L-asparaginazy to enzymy hydrolizujące L-asparaginę do L-asparaginianu oraz amoniaku. Enzymy te dzielą się na trzy klasy strukturalne, jednak tylko asparaginazy klasy pierwszej, dzięki swojemu silnemu oddziaływaniu z L-asparaginą, są wykorzystywane z powodzeniem w terapii białaczki. Komórki nowotworowe są zależne od zewnętrznego źródła L-asparaginy i wymagają dostaw tego aminokwasu z surowicy krwi do swojego wzrostu i podziału. Efekt terapeutyczny L-asparaginazy polega na obniżeniu poziomu L-asparaginy w krwi pacjenta, prowadząc do zahamowania wzrostu komórek nowotworowych. Obecnie w terapii onkologicznej zatwierdzone są jedynie enzymy z dwóch źródeł organizmów bakteryjnych, z Erwinia chrysanthemi (ErAII) oraz Escherichia coli (EcAII). Ostatnie badania sugerują, że potencjał terapeutyczny L-asparaginaz nie ogranicza się jedynie do białaczek i można je zastosować w leczeniu innych typów nowotworów, np. chłoniaków, glejaków czy nowotworów trzustki. Istnieje zatem duże zainteresowanie projektowaniem nowych terapeutycznych L-asparaginaz. Dodatkową motywacją jest również fakt, że stosowane obecnie terapeutyki (ErAII oraz EcAII) mimo swojej skuteczności wywołują również wiele skutków ubocznych.
W projekcie opracowano i stworzono linię obliczeniową do identyfikacji L-asparaginaz, przewidywania ich struktur przestrzennych i analizowania właściwości, zwłaszcza powinowactwa L-asparaginy, w porównaniu z enzymami stosowanymi obecnie w terapii nowotworowej. Opracowane narzędzie umożliwia identyfikację sekwencji L asparaginaz w genomowych bazach danych, generując trójwymiarowe modele wytypowanych białek, a następnie wykorzystuje techniki dokowania, dynamiki molekularnej i chemii kwantowej do oszacowania względnego powinowactwa tych białek do L-asparaginy. Zaawansowana infrastruktura obliczeniowa Poznańskiego Centrum Superkomputerowo-Sieciowego pozwoliła zastosować rozwinięte oprogramowanie do analizy ponad 256 mln białek zawartych w 85 tys. genomów bakteryjnych. Dzięki tym badaniom udało się zidentyfikować kilkaset enzymów o potencjalnie wyższym powinowactwie do substratu niż obecnie stosowane w terapii. Wybrane enzymy wytypowane na podstawie metod obliczeniowych zostaną wyprodukowane w prokariotycznym systemie ekspresyjnym, oczyszczone za pomocą technik chromatograficznych, a następnie ich powinowactwo do substratu zostanie sprawdzone in vitro. Enzymy o najlepszym powinowactwie do L-asparaginazy i odpowiednich parametrach fizykochemicznych będą testowane na wybranych liniach ludzkich komórek nowotworowych w celu oceny ich zdolności do hamowania proliferacji i indukowania apoptozy w tych komórkach, co będzie pierwszym krokiem do ich wykorzystania w terapii.
dr Maciej Janicki
Pracownia Biotechnologii, Wydział Biologii UAM
dr Andrzej Zieleziński
Zakład Biologii Obliczeniowej, Wydział Biologii UAM
dr hab. Joanna Loch
Zakład Krystalochemii i Krystalofizyki, Wydział Chemii UJ
Poznańska Mapa Zero Waste wyróżniona w konkursie Skrzydła IT w Administracji
2026-04-16
Poznańska Mapa Zero Waste, stworzona w ramach współpracy Miasta Poznania i PCSS, otrzymała wyróżnienie w prestiżowym konkursie Skrzydła IT w Administracji. Projekt został doceniony w kategorii „e-Usługi dla obywatela” jako wzór wdrożenia nowoczesnych technologii wspierających ideę gospodarki obiegu zamkniętego. To kolejne potwierdzenie skuteczności synergii między nauką a samorządem w procesie cyfrowej transformacji stolicy Wielkopolski.
System Piast-Q oficjalnie uruchomiony!
2026-04-14
Z okazji World Quantum Day ogłoszono kluczowy krok w rozwoju technologii kwantowych w Polsce i Europie. System komputerowy Piast-Q pomyślnie przeszedł procedury odbioru i został oficjalnie uruchomiony w Poznańskim Centrum Superkomputerowo-Sieciowym. Oznacza to pełną gotowość jednostki do realizacji zaawansowanych operacji obliczeniowych.
Przedstawicielki PCSS w Radzie Pracodawców Collegium da Vinci
2026-03-27
Rada Pracodawców Collegium Da Vinci w Poznaniu to doradczy organ uczelni, w skład którego wchodzą przedstawiciele biznesu, pomagający dostosować programy kształcenia do aktualnych wymagań rynku pracy. Uczelnia stawia na współpracę z praktykami, by zapewnić wysoki wskaźnik zatrudnienia. Do Rady powołano Urszulę Grygier-Soboń, Zastępczynię Pełnomocnika Dyrektora ICHB PAN ds. PCSS oraz dr Magdalenę Baranowską-Szczepańską z Działu Współpracy i Kontaktów z Otoczeniem.
Sieć PIONIER: uruchomiono połączenie z Vienna Internet eXchange
2026-03-25
W minionym tygodniu oficjalnie uruchomiono nowe połączenie sieci PIONIER z punktem wymiany ruchu VIX (Vienna Internet eXchange) w Wiedniu, co stanowi strategiczny krok w rozwoju polskiej infrastruktury sieciowej. Ta kluczowa inwestycja otwiera drogę do bezpośredniej wymiany danych z ponad 180 globalnymi operatorami i dostawcami treści, znacząco wzmacniając pozycję rodzimej nauki oraz gospodarki cyfrowej w europejskim ekosystemie IT.
PIONIER-Q: Budowa transgranicznych połączeń szyfrującego klucza kwantowego
2026-03-24
Zakończono kluczowy etap budowy ogólnopolskiej infrastruktury klucza kwantowego, łączącej centra Komputerów Dużej Mocy w ramach sieci PIONIER. Podczas marcowego spotkania z Komisją Europejską pomyślnie podsumowano wyniki testów oraz zaprezentowano strategię dalszej rozbudowy połączeń o charakterze transgranicznym.
Powstaje nowoczesna infrastruktura kwantowa łącząca Niemcy, Polskę i Czechy
2026-03-20
W marcu ruszył projekt QKD Network Germany‑Poland‑Czechia, który zakłada stworzenie bezpiecznej, odpornej na ataki infrastruktury kwantowej (QCI), która połączy trzy państwa naszego regionu. Będzie to pierwsza w Europie Środkowej tak rozbudowana sieć wykorzystująca Quantum Key Distribution (QKD) – technologię generowania i dystrybucji kluczy kryptograficznych, odporną nawet na przyszłe zagrożenia wynikające z użycia komputerów kwantowych. Inicjatywa wzmacnia cyberbezpieczeństwo państw, zapewniając bezpieczną komunikację pomiędzy instytucjami publicznymi, operatorami infrastruktury krytycznej, sektorem naukowym i centrami danych. Jednym z partnerów projektu jest PCSS.
GraviQ: Budowa pierwszej w Polsce sieci mobilnych grawimetrów kwantowych
2026-03-13
Rozpoczęto realizację projektu GraviQ, którego celem jest wytworzenie innowacyjnej infrastruktury badawczej opartej na zjawiskach mechaniki kwantowej. Inicjatywa zakłada budowę oraz wdrożenie pierwszej w kraju synchronicznej sieci mobilnych grawimetrów kwantowych, co otworzy nowe możliwości w zakresie precyzyjnego monitoringu pola grawitacyjnego Ziemi oraz detekcji zagrożeń naturalnych.
„Bliżej Teatru”: innowacyjny model digitalizacji dziedzictwa scenicznego
2026-03-09
Teatr Polski we Wrocławiu, Poznańskie Centrum Superkomputerowo-Sieciowe oraz Uniwersytet Wrocławski rozpoczęły współpracę nad stworzeniem wzorcowego systemu cyfryzacji teatralnych archiwów artystycznych. Celem projektu jest nie tylko zabezpieczenie unikatowych zbiorów dokumentujących ponad 600 realizacji powstałych od 1945 roku, ale także opracowanie innowacyjnej usługi cyfrowej dla instytucji kultury w całej Polsce.
Quantum Dev Pizza powraca: majowe spotkanie społeczności kwantowej
2026-04-27
Kolejna edycja wydarzenia Quantum Dev Pizza odbędzie się 7 maja 2026 roku o godzinie 18:00 na Uniwersytecie Ekonomicznym w Poznaniu, w sali 1.1 budynku D. Spotkanie jest skierowane do wszystkich osób zainteresowanych technologiami kwantowymi, które chcą poszerzyć swoją wiedzę oraz poznać lokalną społeczność ekspercką. W ramach wieczoru zaplanowano dwie prelekcje merytoryczne oraz czas na networking w luźnej atmosferze przy pizzy.
Rola technologii podwójnego zastosowania w obronności tematem debaty podczas Kongresu INSECON
2026-04-17
15-16 kwietnia 2026 roku odbyła się kolejna edycja Międzynarodowego Kongresu Cyberbezpieczeństwa i Technologii Przełomowych INSECON, będącego jednym z najważniejszych spotkań ekspertów IT w Europie Środkowo-Wschodniej. Wydarzenie to, organizowane przez Ministerstwo Obrony Narodowej, skoncentrowało się na budowaniu świadomości zagrożeń w cyberprzestrzeni oraz prezentacji innowacyjnych rozwiązań zwiększających bezpieczeństwo na poziomie krajowym i międzynarodowym.
Dyrektor Robert Pękal gościem konferencji „Strategie Wzrostu 2026”
2026-04-16
16 kwietnia 2026 roku w siedzibie Urzędu Marszałkowskiego Województwa Wielkopolskiego odbyła się konferencja „Strategie Wzrostu 2026”, stanowiąca platformę wymiany doświadczeń między światem biznesu, administracji i technologii. Wydarzenie, zorganizowane we współpracy z Niderlandzko-Polską Izbą Gospodarczą, skoncentrowało się na wyznaczaniu kluczowych kierunków rozwoju regionu w obliczu dynamicznych zmian rynkowych.
Polish Living Lab Summit w PCSS
2026-04-10
Zorganizowany w siedzibie PCSS (9.04.2026 r.) Polish Living Lab Summit stanowił istotne forum wymiany doświadczeń, potwierdzając kluczową rolę idei współtworzenia w procesie wdrażania nowoczesnych rozwiązań. Wydarzenie zgromadziło szerokie grono ekspertów, partnerów oraz praktyków, stając się przestrzenią do merytorycznego dialogu nad przyszłością innowacji społecznych i technologicznych w Polsce.
Bezpieczeństwo sieci 5G w centrum debaty ekspertów
2026-04-02
1 kwietnia br. w siedzibie Naukowej i Akademickiej Sieci Komputerowej (NASK) odbyły się warsztaty poświęcone wyzwaniom i perspektywom cyberbezpieczeństwa w infrastrukturze telekomunikacyjnej nowej generacji. Wydarzenie zrealizowane w ramach europejskiego projektu 5G-TACTIC stanowiło platformę wymiany wiedzy między sektorem nauki, administracji publicznej oraz przemysłu.
Kwantowa granica jakości: PCSS na XXIX Poznańskim Festiwalu Nauki i Sztuki
2026-04-01
Podczas nadchodzącej edycji Poznańskiego Festiwalu Nauki i Sztuki zaprezentowane zostaną technologie, w których precyzja i bezpieczeństwo wynikają bezpośrednio z fundamentalnych praw fizyki. Poznańskie Centrum Superkomputerowo-Sieciowe przygotowało specjalną ekspozycję ukazującą, jak mechanika kwantowa redefiniuje współczesne standardy inżynierii. Wydarzenie odbędzie się już 22 kwietnia 2026 roku w zabytkowych przestrzeniach Pałacu Działyńskich.
Zapraszamy na AI Tinkerers Poland – Meetup in Poznan #1
2026-03-30
22 kwietnia br. Poznańskie Centrum Superkomputerowo-Sieciowe stanie się miejscem spotkania pasjonatów i praktyków sztucznej inteligencji w ramach wydarzenia AI Tinkerers Poland Poznań #1. Inicjatywa ta skierowana jest do inżynierów oraz naukowców, dla których praca z technologiami LLM i uczeniem maszynowym stanowi przestrzeń do stałego eksperymentowania i innowacji.
Zapraszamy na Polish Living Lab Summit w PCSS
2026-03-27
Jak skutecznie wdrażać innowacje w sektorze publicznym i pozyskiwać środki na projekty o wysokim potencjale społecznym? Już 9 kwietnia Poznańskie Centrum Superkomputerowo-Sieciowe stanie się centrum ogólnopolskiego dialogu między nauką, biznesem a administracją w ramach Polish Living Lab Summit. Serdecznie zapraszamy di udziału w tym wydarzeniu.
PCSS Talks. PUCHACZ: Cyberbezpieczeństwo Polski w szponach sowy
2026-04-23
Najnowszy odcinek podcastu PCSS Talks poświęcony został projektowi PUCHACZ (Platforma Uzyskiwania CHarakterystyk Adwersarzy i CyberZagrożeń), który stanowi jeden z najważniejszych filarów nowoczesnego cyberbezpieczeństwa w Polsce. Rozmowa przybliża założenia tej unikalnej infrastruktury oraz analizuje jej kluczowe znaczenie dla rozwoju krajowej gospodarki i świata nauki.
PCSS Talks: Sztuka pod lupą nauki, czyli jak E-RIHS zmienia badania dziedzictwa kulturowego
2026-03-26
W kolejnym odcinku PCSS Talks odkrywamy kulisy projektu, który łączy humanistów i inżynierów, artystów i chemików, ale ma wpływ na wszystkich, którzy oglądają i podziwiają dzieła sztuki. Z prof. dr. hab. Piotrem Targowskim z Wydziału Fizyki, Astronomii i Informatyki Stosowanej Uniwersytetu Mikołaja Kopernika w Toruniu oraz dr Ewą Kuśmierek z Poznańskiego Centrum Superkomputerowo-Sieciowego, rozmawiają Magdalena Baranowska-Szczepańska i Kacper Zieleniak.
Associated Press: PCSS filarem technologicznej transformacji
2026-03-17
Od postkomunizmu do grona 20 największych gospodarek świata – agencja Associated Press w swoim najnowszym materiale analizuje imponującą transformację Polski. Kluczowym elementem tej ewolucji, obok edukacji i przemysłu, są innowacje, które w materiale AP reprezentuje Poznańskie Centrum Superkomputerowo-Sieciowe.
Udostępniamy technologię AI: Duże modele językowe na wyciągnięcie ręki
2026-03-03
Dostęp do modeli sztucznej inteligencji poprzez interfejs API to usługa PCSS, z której mogą korzystać już nie tylko naukowcy. Początkowo stworzona została ona z myślą o wsparciu badań, projektów akademickich oraz działalności dydaktycznej – ale teraz jest już dostępna komercyjnie! Zaawansowane narzędzia oparte o najnowocześniejszą i – co istotne – bezpiecznej infrastrukturze HPC PCSS są dosłownie na wyciągnięcie ręki także dla przedstawicieli biznesu.
PCSS Talks: PIAST-AI fabryka, w której produkujemy sztuczną inteligencję
2026-02-26
Czym jest fabryka AI i czy faktycznie przypomina linię produkcyjną? W PCSS Talks odkrywamy kulisy projektu PIAST-AI – fundamentu polskiej suwerenności cyfrowej. O surowcach w postaci danych, superkomputerowych „mięśniach” i budowaniu cyfrowych podwalin rozmawiamy z Tomaszem Parkołą, kierownikiem projektu oraz jego zastępczynią, Joanną Kowalską. Poznaj miejsce, gdzie idea zmienia się w gotowe modele sztucznej inteligencji.
Piszą o nas: Praktyczne wdrażanie rodzimych modeli językowych
2026-02-22
W ramach cyklu „Start z polskim AI”, realizowanego przez Polski Fundusz Rozwoju (PFR), ukazała się rozmowa poświęcona implementacji lokalnych rozwiązań sztucznej inteligencji w organizacjach. Gościem spotkania był Tomasz Parkoła, kierownik Pionu Usług Sieciowych PCSS, który przybliżył kulisy pracy z modelem Bielik.AI. Materiał stanowi kompendium wiedzy dla podmiotów planujących strategiczne wdrożenia AI oparte na polskich zasobach.
PCSS Talks: DARIAH – Fuzja humanizmu i technologii
2026-01-29
W pierwszym odcinku podcastu PCSS Talks w 2026 roku zapraszamy na spotkanie z Dominikiem Purchałą, wicedyrektorem Centrum Kompetencji Cyfrowych Uniwersytetu Warszawskiego oraz Maciejem Głowiakiem, kierownikiem Działu Nowych Mediów w naszym Centrum. Magdalena Baranowska-Szczepańska i Kacper Zieleniak rozmawiają z gośćmi o humanistyce cyfrowej – a konkretnie o projekcie DARIAH łączącym technologię z naukami humanistycznymi i sztuką.
Ekspert PCSS współautorem publikacji naukowej w prestiżowym tytule, dot. modułowej architektury referencyjnej SHOP4CF
2026-01-28
Artykuł „The SHOP4CF modular reference architecture for flexible process-oriented, data-driven smart manufacturing” autorstwa: Paula Grefena, Michała Zimniewicza (PCSS, Dział Aplikacji i Usług Wielkiej Skali), Irene Vanderfeesten, Kostasa Traganosa, Pietera Becue, Andersa Pedersena oraz Genessis Perez Rivery ukazał się na łamach 85. numeru „Journal of Manufacturing Systems”, publikowanego na witrynie „ScienceDirect”.
Poznańska Mapa Zero Waste wyróżniona w konkursie Skrzydła IT w Administracji
2026-04-16
Poznańska Mapa Zero Waste, stworzona w ramach współpracy Miasta Poznania i PCSS, otrzymała wyróżnienie w prestiżowym konkursie Skrzydła IT w Administracji. Projekt został doceniony w kategorii „e-Usługi dla obywatela” jako wzór wdrożenia nowoczesnych technologii wspierających ideę gospodarki obiegu zamkniętego. To kolejne potwierdzenie skuteczności synergii między nauką a samorządem w procesie cyfrowej transformacji stolicy Wielkopolski.
Quantum Dev Pizza powraca: majowe spotkanie społeczności kwantowej
2026-04-27
Kolejna edycja wydarzenia Quantum Dev Pizza odbędzie się 7 maja 2026 roku o godzinie 18:00 na Uniwersytecie Ekonomicznym w Poznaniu, w sali 1.1 budynku D. Spotkanie jest skierowane do wszystkich osób zainteresowanych technologiami kwantowymi, które chcą poszerzyć swoją wiedzę oraz poznać lokalną społeczność ekspercką. W ramach wieczoru zaplanowano dwie prelekcje merytoryczne oraz czas na networking w luźnej atmosferze przy pizzy.
PCSS Talks. PUCHACZ: Cyberbezpieczeństwo Polski w szponach sowy
2026-04-23
Najnowszy odcinek podcastu PCSS Talks poświęcony został projektowi PUCHACZ (Platforma Uzyskiwania CHarakterystyk Adwersarzy i CyberZagrożeń), który stanowi jeden z najważniejszych filarów nowoczesnego cyberbezpieczeństwa w Polsce. Rozmowa przybliża założenia tej unikalnej infrastruktury oraz analizuje jej kluczowe znaczenie dla rozwoju krajowej gospodarki i świata nauki.
System Piast-Q oficjalnie uruchomiony!
2026-04-14
Z okazji World Quantum Day ogłoszono kluczowy krok w rozwoju technologii kwantowych w Polsce i Europie. System komputerowy Piast-Q pomyślnie przeszedł procedury odbioru i został oficjalnie uruchomiony w Poznańskim Centrum Superkomputerowo-Sieciowym. Oznacza to pełną gotowość jednostki do realizacji zaawansowanych operacji obliczeniowych.
Rola technologii podwójnego zastosowania w obronności tematem debaty podczas Kongresu INSECON
2026-04-17
15-16 kwietnia 2026 roku odbyła się kolejna edycja Międzynarodowego Kongresu Cyberbezpieczeństwa i Technologii Przełomowych INSECON, będącego jednym z najważniejszych spotkań ekspertów IT w Europie Środkowo-Wschodniej. Wydarzenie to, organizowane przez Ministerstwo Obrony Narodowej, skoncentrowało się na budowaniu świadomości zagrożeń w cyberprzestrzeni oraz prezentacji innowacyjnych rozwiązań zwiększających bezpieczeństwo na poziomie krajowym i międzynarodowym.
PCSS Talks: Sztuka pod lupą nauki, czyli jak E-RIHS zmienia badania dziedzictwa kulturowego
2026-03-26
W kolejnym odcinku PCSS Talks odkrywamy kulisy projektu, który łączy humanistów i inżynierów, artystów i chemików, ale ma wpływ na wszystkich, którzy oglądają i podziwiają dzieła sztuki. Z prof. dr. hab. Piotrem Targowskim z Wydziału Fizyki, Astronomii i Informatyki Stosowanej Uniwersytetu Mikołaja Kopernika w Toruniu oraz dr Ewą Kuśmierek z Poznańskiego Centrum Superkomputerowo-Sieciowego, rozmawiają Magdalena Baranowska-Szczepańska i Kacper Zieleniak.
Przedstawicielki PCSS w Radzie Pracodawców Collegium da Vinci
2026-03-27
Rada Pracodawców Collegium Da Vinci w Poznaniu to doradczy organ uczelni, w skład którego wchodzą przedstawiciele biznesu, pomagający dostosować programy kształcenia do aktualnych wymagań rynku pracy. Uczelnia stawia na współpracę z praktykami, by zapewnić wysoki wskaźnik zatrudnienia. Do Rady powołano Urszulę Grygier-Soboń, Zastępczynię Pełnomocnika Dyrektora ICHB PAN ds. PCSS oraz dr Magdalenę Baranowską-Szczepańską z Działu Współpracy i Kontaktów z Otoczeniem.
Dyrektor Robert Pękal gościem konferencji „Strategie Wzrostu 2026”
2026-04-16
16 kwietnia 2026 roku w siedzibie Urzędu Marszałkowskiego Województwa Wielkopolskiego odbyła się konferencja „Strategie Wzrostu 2026”, stanowiąca platformę wymiany doświadczeń między światem biznesu, administracji i technologii. Wydarzenie, zorganizowane we współpracy z Niderlandzko-Polską Izbą Gospodarczą, skoncentrowało się na wyznaczaniu kluczowych kierunków rozwoju regionu w obliczu dynamicznych zmian rynkowych.
Associated Press: PCSS filarem technologicznej transformacji
2026-03-17
Od postkomunizmu do grona 20 największych gospodarek świata – agencja Associated Press w swoim najnowszym materiale analizuje imponującą transformację Polski. Kluczowym elementem tej ewolucji, obok edukacji i przemysłu, są innowacje, które w materiale AP reprezentuje Poznańskie Centrum Superkomputerowo-Sieciowe.
Sieć PIONIER: uruchomiono połączenie z Vienna Internet eXchange
2026-03-25
W minionym tygodniu oficjalnie uruchomiono nowe połączenie sieci PIONIER z punktem wymiany ruchu VIX (Vienna Internet eXchange) w Wiedniu, co stanowi strategiczny krok w rozwoju polskiej infrastruktury sieciowej. Ta kluczowa inwestycja otwiera drogę do bezpośredniej wymiany danych z ponad 180 globalnymi operatorami i dostawcami treści, znacząco wzmacniając pozycję rodzimej nauki oraz gospodarki cyfrowej w europejskim ekosystemie IT.
Polish Living Lab Summit w PCSS
2026-04-10
Zorganizowany w siedzibie PCSS (9.04.2026 r.) Polish Living Lab Summit stanowił istotne forum wymiany doświadczeń, potwierdzając kluczową rolę idei współtworzenia w procesie wdrażania nowoczesnych rozwiązań. Wydarzenie zgromadziło szerokie grono ekspertów, partnerów oraz praktyków, stając się przestrzenią do merytorycznego dialogu nad przyszłością innowacji społecznych i technologicznych w Polsce.
Udostępniamy technologię AI: Duże modele językowe na wyciągnięcie ręki
2026-03-03
Dostęp do modeli sztucznej inteligencji poprzez interfejs API to usługa PCSS, z której mogą korzystać już nie tylko naukowcy. Początkowo stworzona została ona z myślą o wsparciu badań, projektów akademickich oraz działalności dydaktycznej – ale teraz jest już dostępna komercyjnie! Zaawansowane narzędzia oparte o najnowocześniejszą i – co istotne – bezpiecznej infrastrukturze HPC PCSS są dosłownie na wyciągnięcie ręki także dla przedstawicieli biznesu.
PIONIER-Q: Budowa transgranicznych połączeń szyfrującego klucza kwantowego
2026-03-24
Zakończono kluczowy etap budowy ogólnopolskiej infrastruktury klucza kwantowego, łączącej centra Komputerów Dużej Mocy w ramach sieci PIONIER. Podczas marcowego spotkania z Komisją Europejską pomyślnie podsumowano wyniki testów oraz zaprezentowano strategię dalszej rozbudowy połączeń o charakterze transgranicznym.
Bezpieczeństwo sieci 5G w centrum debaty ekspertów
2026-04-02
1 kwietnia br. w siedzibie Naukowej i Akademickiej Sieci Komputerowej (NASK) odbyły się warsztaty poświęcone wyzwaniom i perspektywom cyberbezpieczeństwa w infrastrukturze telekomunikacyjnej nowej generacji. Wydarzenie zrealizowane w ramach europejskiego projektu 5G-TACTIC stanowiło platformę wymiany wiedzy między sektorem nauki, administracji publicznej oraz przemysłu.
PCSS Talks: PIAST-AI fabryka, w której produkujemy sztuczną inteligencję
2026-02-26
Czym jest fabryka AI i czy faktycznie przypomina linię produkcyjną? W PCSS Talks odkrywamy kulisy projektu PIAST-AI – fundamentu polskiej suwerenności cyfrowej. O surowcach w postaci danych, superkomputerowych „mięśniach” i budowaniu cyfrowych podwalin rozmawiamy z Tomaszem Parkołą, kierownikiem projektu oraz jego zastępczynią, Joanną Kowalską. Poznaj miejsce, gdzie idea zmienia się w gotowe modele sztucznej inteligencji.
Powstaje nowoczesna infrastruktura kwantowa łącząca Niemcy, Polskę i Czechy
2026-03-20
W marcu ruszył projekt QKD Network Germany‑Poland‑Czechia, który zakłada stworzenie bezpiecznej, odpornej na ataki infrastruktury kwantowej (QCI), która połączy trzy państwa naszego regionu. Będzie to pierwsza w Europie Środkowej tak rozbudowana sieć wykorzystująca Quantum Key Distribution (QKD) – technologię generowania i dystrybucji kluczy kryptograficznych, odporną nawet na przyszłe zagrożenia wynikające z użycia komputerów kwantowych. Inicjatywa wzmacnia cyberbezpieczeństwo państw, zapewniając bezpieczną komunikację pomiędzy instytucjami publicznymi, operatorami infrastruktury krytycznej, sektorem naukowym i centrami danych. Jednym z partnerów projektu jest PCSS.
Kwantowa granica jakości: PCSS na XXIX Poznańskim Festiwalu Nauki i Sztuki
2026-04-01
Podczas nadchodzącej edycji Poznańskiego Festiwalu Nauki i Sztuki zaprezentowane zostaną technologie, w których precyzja i bezpieczeństwo wynikają bezpośrednio z fundamentalnych praw fizyki. Poznańskie Centrum Superkomputerowo-Sieciowe przygotowało specjalną ekspozycję ukazującą, jak mechanika kwantowa redefiniuje współczesne standardy inżynierii. Wydarzenie odbędzie się już 22 kwietnia 2026 roku w zabytkowych przestrzeniach Pałacu Działyńskich.
Piszą o nas: Praktyczne wdrażanie rodzimych modeli językowych
2026-02-22
W ramach cyklu „Start z polskim AI”, realizowanego przez Polski Fundusz Rozwoju (PFR), ukazała się rozmowa poświęcona implementacji lokalnych rozwiązań sztucznej inteligencji w organizacjach. Gościem spotkania był Tomasz Parkoła, kierownik Pionu Usług Sieciowych PCSS, który przybliżył kulisy pracy z modelem Bielik.AI. Materiał stanowi kompendium wiedzy dla podmiotów planujących strategiczne wdrożenia AI oparte na polskich zasobach.
GraviQ: Budowa pierwszej w Polsce sieci mobilnych grawimetrów kwantowych
2026-03-13
Rozpoczęto realizację projektu GraviQ, którego celem jest wytworzenie innowacyjnej infrastruktury badawczej opartej na zjawiskach mechaniki kwantowej. Inicjatywa zakłada budowę oraz wdrożenie pierwszej w kraju synchronicznej sieci mobilnych grawimetrów kwantowych, co otworzy nowe możliwości w zakresie precyzyjnego monitoringu pola grawitacyjnego Ziemi oraz detekcji zagrożeń naturalnych.
Zapraszamy na AI Tinkerers Poland – Meetup in Poznan #1
2026-03-30
22 kwietnia br. Poznańskie Centrum Superkomputerowo-Sieciowe stanie się miejscem spotkania pasjonatów i praktyków sztucznej inteligencji w ramach wydarzenia AI Tinkerers Poland Poznań #1. Inicjatywa ta skierowana jest do inżynierów oraz naukowców, dla których praca z technologiami LLM i uczeniem maszynowym stanowi przestrzeń do stałego eksperymentowania i innowacji.
PCSS Talks: DARIAH – Fuzja humanizmu i technologii
2026-01-29
W pierwszym odcinku podcastu PCSS Talks w 2026 roku zapraszamy na spotkanie z Dominikiem Purchałą, wicedyrektorem Centrum Kompetencji Cyfrowych Uniwersytetu Warszawskiego oraz Maciejem Głowiakiem, kierownikiem Działu Nowych Mediów w naszym Centrum. Magdalena Baranowska-Szczepańska i Kacper Zieleniak rozmawiają z gośćmi o humanistyce cyfrowej – a konkretnie o projekcie DARIAH łączącym technologię z naukami humanistycznymi i sztuką.
„Bliżej Teatru”: innowacyjny model digitalizacji dziedzictwa scenicznego
2026-03-09
Teatr Polski we Wrocławiu, Poznańskie Centrum Superkomputerowo-Sieciowe oraz Uniwersytet Wrocławski rozpoczęły współpracę nad stworzeniem wzorcowego systemu cyfryzacji teatralnych archiwów artystycznych. Celem projektu jest nie tylko zabezpieczenie unikatowych zbiorów dokumentujących ponad 600 realizacji powstałych od 1945 roku, ale także opracowanie innowacyjnej usługi cyfrowej dla instytucji kultury w całej Polsce.
Zapraszamy na Polish Living Lab Summit w PCSS
2026-03-27
Jak skutecznie wdrażać innowacje w sektorze publicznym i pozyskiwać środki na projekty o wysokim potencjale społecznym? Już 9 kwietnia Poznańskie Centrum Superkomputerowo-Sieciowe stanie się centrum ogólnopolskiego dialogu między nauką, biznesem a administracją w ramach Polish Living Lab Summit. Serdecznie zapraszamy di udziału w tym wydarzeniu.
Ekspert PCSS współautorem publikacji naukowej w prestiżowym tytule, dot. modułowej architektury referencyjnej SHOP4CF
2026-01-28
Artykuł „The SHOP4CF modular reference architecture for flexible process-oriented, data-driven smart manufacturing” autorstwa: Paula Grefena, Michała Zimniewicza (PCSS, Dział Aplikacji i Usług Wielkiej Skali), Irene Vanderfeesten, Kostasa Traganosa, Pietera Becue, Andersa Pedersena oraz Genessis Perez Rivery ukazał się na łamach 85. numeru „Journal of Manufacturing Systems”, publikowanego na witrynie „ScienceDirect”.